Für Menschen mit chronischer lymphatischer Leukämie (CLL) ist es besonders wichtig, Infektionen zu vermeiden. Denn häufig ist ihr Immunsystem geschwächt. Das erhöht die Infektneigung und das Risiko für schwere Verläufe.
Entsprechend bedeutsam ist es für sie, ihren Impfschutz aktuell zu halten. Vor Beginn der Grippewelle ist ein guter Zeitpunkt, ihn zu checken und zu ergänzen.
Wieso kann die Infektneigung bei Menschen mit CLL erhöht sein?
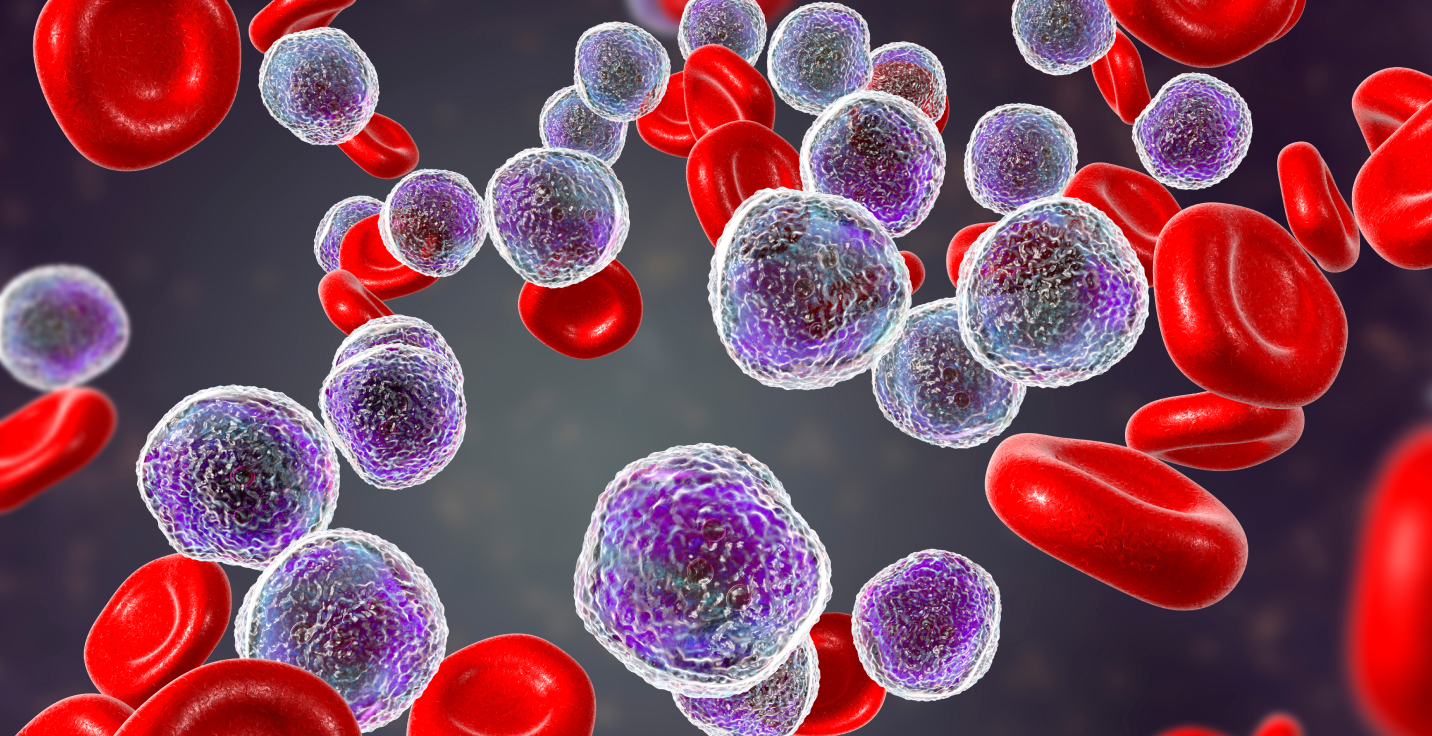
Die Gründe können in der Erkrankung selbst und auch in der Therapie liegen. Gesunde B-Lymphozyten (B-Zellen) spielen bei der Abwehr von Infektionen eine wichtige Rolle. Bei der CLL kommt es zu einer unkontrollierten Vermehrung von abnormalen B-Lymphozyten, die diese Funktion nur noch eingeschränkt wahrnehmen. Bei einer fortschreitenden CLL wächst die Zahl der veränderten B-Zellen so weit an, dass sie die gesunden B-Zellen in bestimmten Bereichen immer mehr verdrängen – und somit die Immunabwehr schwächen.
Hinzu kommt, dass bei CLL gängige Behandlungen – wie insbesondere die zielgerichteten Therapien – die körpereigene Abwehr zusätzlich unterdrücken können. Mehr Infos
Sollten sich Menschen mit CLL jährlich gegen Grippe (Influenza) impfen lassen?
Ja. Das empfiehlt die medizinische S3-Leitlinie zur Behandlung der CLL.
Bekommen Ältere einen anderen Influenzaimpfstoff?
Ja. Die Ständige Impfkommission (STIKO) am Robert Koch-Institut (RKI) empfiehlt, ab der Influenza-Saison 2025/2026 alle Personen im Alter ab 60 Jahren entweder mit einem wirkverstärkten Impfstoff (MF59-adjuvantierter Influenzaimpfstoff) oder einem Hochdosis-Influenzaimpfstoff zu impfen.
Der MF59-adjuvantierte Influenzaimpfstoff (zugelassen ab 50 Jahren) enthält sogenannte Adjuvantien (Hilfsstoffe), die die Wirkung verstärken. Der Hochdosis-Impfstoff (zugelassen ab 60 Jahren) enthält eine höhere Menge Antigen, also jener Virus-Bestandteile
Laut RKI haben sowohl der Hochdosis- als auch der MF-59-adjuvantierte Influenza-Impfstoff im Vergleich zu inaktivierten, Influenza-Standard-Impfstoffen eine geringfügig aber signifikant bessere Wirksamkeit bei Personen ab 60 Jahren.
Wann sollte die Grippe-Impfung am besten stattfinden?
Um rechtzeitig zu Beginn der Grippewelle geschützt zu sein, empfiehlt das RKI die Influenzaimpfung ab Oktober bis Mitte Dezember.
Welche Nebenwirkungen sind bei Influenzaimpfstoffen möglich?
Der Influenzaimpfstoff ist in der Regel gut verträglich. Da sich das Immunsystem mit dem Impfstoff auseinandersetzt, kann es zu vorübergehenden Impfreaktionen kommen – meist sind es Beschwerden wie bei einer Erkältung: Es können zum Beispiel Fieber, Frösteln oder Schwitzen, Müdigkeit, Kopf-, Muskel- oder Gliederschmerzen auftreten. An der Einstichstelle kann es zu leichten Schmerzen, beziehungsweise einer Rötung und Schwellung kommen.
In der Regel klingen die Beschwerden jedoch innerhalb von ein bis zwei Tagen wieder ab.
Beim Hochdosis-Impfstoff gegen Influenza können vermehrt lokale Nebenwirkungen an der Injektionsstelle (Schmerz, Rötung, Schwellung) auftreten. Auch diese Beschwerden sollten nach einigen Tagen von selbst verschwinden.
Wenn man sich gleichzeitig gegen Influenza und COVID-19 impfen lässt, können Impfreaktionen häufiger und eventuell intensiver auftreten als bei der getrennten Gabe der Impfstoffe.
Wird CLL-Patient:innen eine jährliche Impfung gegen COVID-19 empfohlen?
Die S3-Leitlinie zur Behandlung der CLL empfiehlt allen Menschen mit CLL grundsätzlich die Impfung gegen COVID-19 und die jährliche Auffrischungsimpfung.
Dabei sollte allerdings ein zeitlicher Abstand zur letzten COVID-19-Infektion eingehalten werden. Wenn Sie in den vergangenen Monaten an COVID-19 erkrankt waren, sollten Sie dies vor der Impfung erwähnen. Ob, beziehungsweise wann dann geimpft wird, ist eine ärztliche Einzelfallentscheidung.
Wieso werden gegen Grippe und COVID-19 jährliche Impfungen angeboten?
Influenzaviren verändern sich ständig und bilden neue Varianten. Das gilt auch für die Coronaviren (Fachbegriff SARS-CoV-2). Dadurch besteht die Möglichkeit, dass sich Menschen im Laufe ihres Lebens mehrfach mit Grippe und COVID-19 anstecken und erkranken. Daher ist es gerade für Menschen mit höherem Risiko für einen schweren Verlauf wichtig, ihren Impfschutz jährlich aufzufrischen.
Die Impfstoffe gegen Grippe und COVID-19 werden jährlich angepasst, entsprechend der voraussichtlich ab Herbst zirkulierenden Virus-Varianten. Die aktuellen Influenza-Impfstoffe richten sich gegen bestimmte Viren aus den Influenza-A- und Influenza-B-Virus-Stämmen. Die aktuellen COVID-19-Impfstoffe richten sich gegen Viren aus verschiedenen Untergruppen der Omikron-Variante.
Welche Impfungen sind noch wichtig?
Darüber, welche Impfungen Sie noch benötigen, und welcher Impfschutz aufgefrischt werden sollte, sprechen Sie am besten mit Ihrem Arzt oder Ihrer Ärztin. Die Entscheidung hängt von unterschiedlichen Faktoren ab. Wichtig sind unter anderem Ihr Alter und bereits erfolgte Impfungen.
Möglicherweise sind für Sie zum Beispiel Impfungen gegen Pneumokokken und/oder RSV (das Humane Respiratorische Synzytialvirus) nötig.
Pneumokokken können unter anderem schwere Infektionen wie Lungenentzündung, Blutvergiftung oder Hirnhautentzündung verursachen. Eine Infektion mit RSV kann ebenfalls zu einer schweren Lungenentzündung führen.
Weitere Informationen zum Infektionsschutz bei CLL finden Sie in diesem Artikel und in der Broschüre „Wie kann ich mein Immunsystem schützen?“ von AstraZeneca, die Sie hier herunterladen können.
Zusammenfassung
Mit Beginn der kalten Jahreszeit kommt es vermehrt zu Atemwegsinfektionen. Menschen mit CLL haben häufig ein geschwächtes Immunsystem und dadurch ein höheres Risiko für schwere Verläufe. Daher ist jetzt ist ein guter Zeitpunkt für Sie, Ihren Impfschutz zu prüfen und sich mit den für Sie empfohlenen Impfungen besser vor Infektionen zu schützen.